
علاوه برNT، ساير مارکرهاي سونوگرافيک تريمستر اول براي تريزومي 21: عدم وجود استخوان بيني، افزايش امپدانس جريان در داکتوس ونوزوس و رگورژيتاسيون تري کوسپيد است. (جدول 2) نبود استخوان بيني، معکوس شدن موج a در داکتوس ونوزوس و تري کوسپيد رگورژيتاسيون به ترتيب در 60، 66 و 55% جنين هاي تريزومي 21 و در 2.5، 3 و1%متعاقبا در جنين هاي يوپلوئيد مشاهده مي شوند.
ارزيابي هر يک از اين مارکرهاي سونوگرافيک مي تواند در تريمستر اول به همراه اسکرينينگ با سن مادر، NT جنين و سطح سرمي آزاد B-HCG و PAPP-Aبه کار رود تا منجر به بهبود کارايي با افزايش کشف موارد به ميزان 96-93% و کاهش موارد مثبت کاذب تا 2.5% گردد. بهبود کارآيي به ميزان مشابهي در اسکرينينگ يک مرحله اي با سن مادر، NT وسطح سرمي B-HCG و PAPP-A محتمل است به دست آيد. بيماران با ريسک 50/1 يا بيشتر اسکرين مثبت محسوب مي شوند و آنهايي که ريسک کمتر از 1000/1 دارند اسکرين منفي مي باشند. بيماران با ريسک متوسط 1000/1-51/1 شامل 15% جمعيت کلي هستند که وارد اسکرينينگ مرحله دوم مي گردند و به وسيله Nasal Bone، داکتوس ونوزوس يا جريان خون تري کوسپيد ريسک مرحله اول آنها تغيير مي يابد.
مارکر ديگري که اخيرا در تريمستر اول براي تريزومي 21 شرح داده شده افزايش جريان در شريان هپاتيک است. اين مارکر نيز محتمل است در گروه ريسک متوسط پس از اسکرينينگ مرحله اول کاربردي داشته باشد.
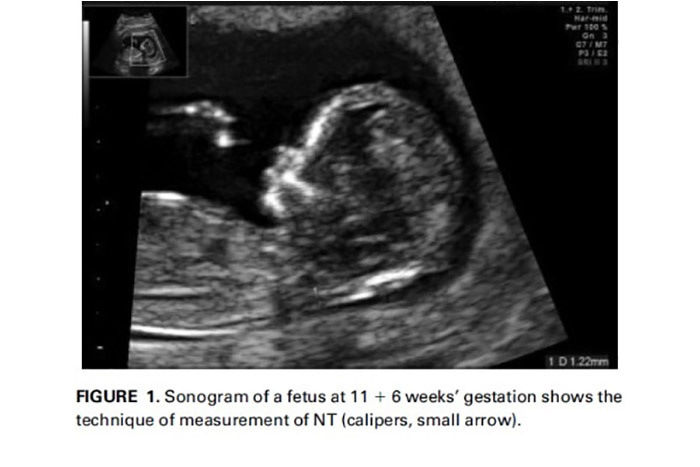
بهترين اسکرينينگ تريمستر اول، به وسيله ترکيبي از سن مادر، تست هاي بيوشيميايي سرمي و مارکرهاي سونوگرافيک متعدد به دست مي آيد.با ريسک 100/1 تشخيص تريزومي 21، 95% و موارد مثبت کاذب 5/2% است. اين کارايي با اين سياست نيز به دست مي آيد که تست هاي بيوشيميايي در کليه بيماران انجام گيرد يا در مرحله اول اسکرينينگ بسته به سن مادر NT و همچنين فلوي تري کوسپيد و داکتوس ونوزوس اندازه گيري شود و سپس تنها در بيماران با ريسک متوسط تست هاي بيوشيميايي انجام گيرد که 20% موارد کلي راتشکيل مي دهند.
يک روش اسکرينينگ آلترناتيو اين است که در همه بارداري ها، تست هاي سرمي مادر انجام گيرد و سپس NT فقط در گروهي که ريسک متوسطي در تست هاي سرمي داشتند انجام شود. مطالعاتي که کارايي پتانسيل اين روش ها را محاسبه کرده اند ميزان کشف موارد و موارد مثبت کاذب را به ترتيب 90-80% و 6-4% برآورد کرده اند و اندازه گيري NT جنين تنها در 40-20% موارد ضرورت مي يابد. فايده اين روش که تست بيوشيميايي مرحله اول را تشکيل مي دهد سادگي آن است. البته تفسير نتايج بيوشيميايي بستگي به اندازه گيري صحيح CRL جنين دارد و بنابراين انجام سونوگرافي اجتناب ناپذير است.
در مطالعاتي که کارايي پتانسيل تست هاي اسکرينيگ را برآورد مي کنند،CRL جنين توسط يک سونوگرافر آموزش ديده همراه با انجام NT جنين انجام شده واين تصور که انگيزه سونوگرافر و دقت تعيين CRL در صورتي که فقط CRL اندازه گيري شود بالاتر است، اشتباه مي باشد.
بيشترين فوايد انتخاب سونوگرافي به جاي تست هاي بيوشيميايي به عنوان مرحله اول، اولا در اين است که هزينه اسکرينينگ کاملا پايين تر است زيرا در اين صورت افرادي که نياز به انجام تست هاي سرمي free B-HCG و PAPP-A پيدا مي کنند تنها20% کل بارداري ها هستند؛ دوم اينکه آناتومي جنين ارزيابي مي شود که منجر به کشف بسياري آنومالي ها در کل بارداري ها مي گردد؛ سوم اينکه مطالعات داپلر مي تواندبه همراه NT در يک آزمون انجام گردد؛ چهارم اينکه موج a معکوس و رگورژيتاسيون تري کوسپيد تنها در تريزومي 21 مورد استفاده نيست بلکه در انوپلوئيدي هاي ديگر و نقائص قلبي جنين نيز مطرح است اما اشکال اين روش اين است که زمانبر بوده و نياز به سونوگرافر آموزش ديده دارد.
در اسکن تريمستر دوم هر نقص کروموزومي پاترن سندرمي مخصوص به خود از آنومالي هاي قابل تشخيص را دارد. براي مثال تريزومي 21 با نقص قلبي، آترزي دئودنوم، هيپوپلازي نازال، افزايش نوکال فولد، ضخامت پره نازال، کانون هاي اکوژن داخل قلب و روده اکوژن، هيدرونفروز خفيف، کوتاهي فمور و هومروس، sandal gap و هيپوپلازي فالانژ مياني انگشت پنجم همراه است.
در تريزومي 18، يافته هاي شايع شامل سر با نماي Strawberry، کيست کوروئيد پلکسوس، نبود کورپوس کالوزوم، بزرگي سيسترنامگنا، شکاف صورت، ميکروگناتيا، ادم نوکال،نقص قلبي، هرني ديافراگمي، آترزي مري، اگزومفالوس، شريان نافي منفرد، آنومالي کليوي، روده اکوژن، ميلومننگوسل، اختلال رشد، کوتاهي اندام، آپلازي راديال، انگشتان روي هم و پاي Rocker Bottom همراه است.
تريزومي 13، با هولوپروزنسفالي، ميکروسفالي،آنومالي صورت، قلب، کليه هاي اکوژن، اگزومفالوس، پلي داکتيلي پست اگزيال همراه مي باشد.
اگر اسکن تريمستر دوم، آنومالي ماژور نشان دهد حتي اگر ايزوله باشد انجام کاريوتايپ جنين توصيه مي شود و چون شيوع اين آنومالي ها پايين است لذا تاثير هزينه ها کم مي باشد. اگر اين آنومالي ها کشنده يا با موربيديته بالا همراه باشند، مانند هولوپروزنسفالي، اهميت انجام کاريوتيپ در جنين، تعيين علت محتمل و ريسک عود آن است. اگر آنومالي قابليت تصحيح در دوره جنيني يا پس از تولد را داشته باشد مانند هرني هياتال، لازم است نقص کروموزومي زمينه رد شود. به خصوص که با آنومالي هاي کروموزومي بسياري مانند تريزومي 13 و 18 ديده مي شود.
آنومالي هاي جنيني مينور يا Soft Markers شايع هستند و عموما با موربيديته همراهي ندارند، مگر اين كه نقص کروموزومي زمينه اي وجود داشته باشد. تعيين کاريوتايپ به صورت روتين در همه بارداري هاي داراي اين مارکر ها، عوارض ماژور مانند ريسک سقط جنين را دارد و هم چنين پر هزينه است، لذا بهتر است در اين موارد در مورد تخمين ريسک نقص کروموزومي مشورت گردد تا اين تست تهاجمي در موارد لزوم انجام شود. ريسک هر شخص با ضرب ريسکA Priori (براساس نتايج اسکرينيگ بوسيله NT و يا تست هاي بيوشيميايي هم زمان) به وسيله نسبت احتمالي آنومالي اختصاصي يا مارکربه دست مي آيد.
برآورد مي شود که اسکن تريمستر دوم شانس تشخيص تريزومي 21 را نسبت به اسکرينينگ ترکيبي تريمستر اول 6% بهتر مي کندو ريسک مثبت کاذب 1.2% بالاتر مي رود.
سه الگوي محاسباتي در مورد استفاده از تست هاي بيوشيميايي تريمستر دوم با هدف بهبود اسکرينينگ تست هاي ترکيبي طرح ريزي شده است.
اول:
تست Integrated در همه بيماران تست NT و PAPP-A در تريمستر اول و AFP ,U E3, Free BHCG, Inhibin در تريمستر دوم انجام شده است و نتايج ترکيبي محاسبه و بيماران پر خطرتحت آمنيوسنتز تريمستر دوم قرار مي گيرند.
دوم:
اسکرينيگ پله اي که در همه بيماران NT محاسبه وسپس Free BHCG, PAPP-A انجام و در بيماران پر خطرCVS پيشنهاد مي شود و موارد ريسک پايين و متوسط در تريمستر دوم AFP, U E3, Free BHCG, Inhibinانجام مي شود و در صورت ريسک بالا امنيوسنتز تريمستر دوم پيشنهاد مي شود.
سوم:
اسکرينينگ Contingent که شبيه پله اي است اما تست هاي بيوشيميايي فقط در بيماران ريسک متوسط انجام مي گردد.
کارآيي تخميني اين سه روش مشابه و 94-90% و مثبت کاذب 5% است. فايده روش Contingent اين است که در 80-75% موارد تست تريمستر دوم اجتناب مي گردد و همچنين تشخيص 60% آنوپلوئيدي ها در تريمستر اول داده مي شود. اشکال اين روش ها اين است که اولاً کارايي آنها از روش ترکيبي تريمستر اول که مارکرهاي جديد سونوگرافيک را مداخله مي دهد ضعيف تر است، دوم اينکه اطمينان بخشي به والدين کم خطر چند هفته تاخير مي يابد، سوم اين كه بسياري خانم ها با بارداري دچار مشکل، از اختتام بي خطر تر در تريمستر اول محروم مي شوند و چهارم اين كه بسياري خانم ها به علت عدم تکميل تست دو مرحله اي از اسکرينيگ محروم مي شوند.
نتيجه مفيد اسکرينينگ تريزومي 21 تشخيص زودتر تريزومي 18. و 13 نيز هست که به ترتيب دومين و سومين نقائص شايع کروموزومي هستند. در 13-11 هفتگي شيوع نسبي تريزومي هاي 18 و 13 به 21، يک به سه و يک به هفت هستند. همه اين سه نوع تريزومي با افزايش سن مادر و NT وکاهش سرمي PAPP-A مادر همراه هستند. اما در تريزومي 21، Free BHCG افزايش يافته ولي در تريزومي 13 و 18 کاهش مي يابد؛ به علاوه تريزومي 13 برخلاف 18 و 21 با تاکي کاردي و ضربان قلب بالاي صدک 95% در جنين هاي يوپلوئيد همراه است که در 85% موارد تريزومي 13 ديده مي شود.استفاده از الگوريتم تريزومي 21 حدود 75% موارد تريزومي 18 و 13 را هم قابل تشخيص مي کند و ترکيب الگوريتم آن با الگوريتم هاي تريزومي 18 و 13 ميزان تشخيص را به 95% و مثبت کاذب را فقط 0.1% افزايش مي دهد.نتايج مفيد ديگر، سه الگوريتم تشخيص 85% تريپلوئيدي ها است.به علاوه تعيين NT در 13-11 هفتگي کشف بسياري نقائص ماژور مانند هولوپروزنسفالي، اگزومفالوس و مگاسيستيس را در 1300/1، 400/1 و 1600/1 جنين ها متعاقباً تعيين مي کند. آنوپلوئيدي به خصوص تريزومي 18 و 13 در 65% بيماران هولوپروزنسفالي، 55% اگزومفالوس و 30% مگاسيستيس ديده مي شود.در 13-11 هفته، نبود استخوان بيني فلوي غير عادي داکتوس ونوزوس و رگورژيتاسيون تري کوسپيددر 50، 55 و 30% موارد متعاقباً در تريزومي 18 و 13 ديده مي شود.
در دوقلويي، اسکرينينگ موثر با تر کيب سن مادر و NT جنين بدست مي آيد. کارآيي اسکرينينگ با تست هاي بيوشيميايي سرم مادر افزايش مي يابد، اما لازم است که کوريونيسيته مشخص شود در دوقلويي دي کوريوني در 13-11 هفته سطح PAPP-A, Free BHCG حدود دو برابر تک قلويي است اما در مونو کوريون ها ميزان آن کمتر از دي کوريون ها است.
در دوقلوهاي دي کوريوني ريسک مخصوص بيمار در هر جنين بر اساس سن مادر و NT محاسبه مي شود و ميزان تعيين آن 80-75% و مثبت کاذب 5% در هر جنين و 10% د رحاملگي است که شبيه به تک قلويي است.
در محاسبه ريسک تريزومي فرض مي شود که در هر حاملگي تعيين NT براي CRL بين دو جنين مستقل از هم است، البته شواهد اخير بيانگر اين است که در دوقلوهاي يوپلوئيد دي کوريوني تعيين NT هر قل به هم مربوط هستند و اين ارتباط انعکاس ساده اي از اثر شايع سونوگرافر نيست. بنابراين لازم است اين ارتباط محاسبه گردد چون اثر کافي در تعيين ريسک مخصوص هر بيمار دارد. اسکرين تريمستر اول اجازه مي دهد تا در مواردي که يک جنين يوپلوئيد و ديگري آنومال است زودتر و بي خطرتر از فتوسيد استفاده شود.
در منوکوريون ها، مثبت کاذب NT بيش از دي کوريون هاست، چون افزايش NT ممکن است به علت تظاهر زود هنگام ترانسفوزيون يك قل به قل ديگر و يا مارکر يک اختلال کروموزومي باشد. لذا در محاسبه ريسک تريزومي 21 مي بايستNT هر قل تعيين شده و ميانگين دو جنين محاسبه گردد.
1. Malone FD, Canick JA, Ball RH, et al. First- and Second-Trimester Evaluation of Risk (FASTER) Research Consortium. 2005. First-trimester or second trimester screening, or both, for Down’s syndrome. N Engl J Med 353:2001–2011.
2. Nicolaides KH. 2003. Screening for chromosomal defects. Ultrasound Obstet Gynecol 21: 313–321.
3. Nicolaides KH. 2004. Nuchal translucency and other first-trimester sonographic markers of chromosomal abnormalities. Am J Obstet Gynecol 191: 45–67.
4. Nicolaides KH, Azar G, Byrne D, Mansur C, Marks K. 1992a. Fetal nuchal translucency: ultrasound screening for chromosomal defects in first trimester of pregnancy. Br Med J 304: 867–86
5. Snijders RJM, Holzgreve W, Cuckle H, Nicolaides KH. 1994. Maternal agespecific risks for trisomies at 9–14 weeks’ gestation. Prenat Diagn 14: 543–552.
6. Snijders RJM, Sebire NJ, Cuckle H, Nicolaides KH. 1995. Maternal age and gestational age-specific risks for chromosomal defects. Fetal Diagn Ther 10: 356–367.
7. Snijders RJ, Noble P, Sebire N, Souka A, Nicolaides KH. Fetal Medicine Foundation First Trimester Screening Group. 1998. UK multicentre project on assessment of risk of trisomy 21 by maternal age and fetal nuchaltranslucency thickness at 10–14 weeks of gestation. Lancet 352: 343–346.
8. Snijders RJM, Sundberg K, Holzgreve W, Henry G, Nicolaides KH. 1999.
Maternal age and gestation- specific risk for trisomy 21. Ultrasound Obstet Gynecol 13: 167–170.
9. Souka AP, Snidjers RJM, Novakov A, Soares W, Nicolaides KH. 1998. Defects and syndromes in chromosomally normal fetuses with increased nuchal translucency thickness at 10–14 weeks of gestation. Ultrasound Obstet Gynecol 11: 391–400.
10. Souka AP, Pilalis A, Kavalakis Y, et al. 2004. Assessment of fetal anatomy at the 11–13-week ultrasound examination. Ultrasound Obstet Gynecol 24: 730–734.
11. Kypros H. Nicolaides. 2011. Screening for fetal aneuploidies at 11 to 13 weeks. Prenat Diagn 2011; 31: 7–15.